 |
 |
 |
アルツハイマー病アミロイドβペプチド(Aβ)を分解するシステムの同定
神経蛋白制御研究チーム |
 |
 |
研究の背景
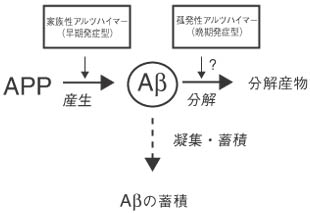
孤発性のアルツハイマー病は、基本的に家族性と同様の病理変化を示し、Aβが蓄積するが、Aβ生成が上昇する証拠は得られていない。合成が上昇しないのに蓄積するということは、分解の低下が原因でないかと推測される(図)。しかし、Aβの生成系についてはすでに詳細に検討されていたのに対して、分解系についてはまったくわかっていなかった。本研究は、このような背景をもとに開始された。
成果
脳内のAβ分解について、2つの方法で調べた。1つは、放射性多重標識した合成Aβを脳内に投与し、その分解過程を高速液体クロマトグラフィーで調べる方法である。もう1つは、非常に感度の高い酵素抗体法を用いて、内在性のAβ存在量
を測定する方法である。その結果、以下の点が明らかになった。
| (1) |
放射性標識Aβの分解が、ネプリライシンノックアウトマウス脳で顕著に減速していた。ネプリライシンが主要なAβ分解酵素であることを示している。
|
| (2) |
ネプリライシンノックアウトマウス脳において、内在性Aβの量
が約2倍に上昇していた。ネプリライシンが内在性Aβの分解を担うことを示している。
|
| (3) |
上記いずれの方法を用いた場合も、ネプリライシン遺伝子が半分だけ欠損しているヘテロのノックアウトマウスにおいて分解の抑制が見られた。脳内Aβの量
は、ネプリライシンの遺伝子量に逆相関していた。これは、脳内のネプリライシン活性が部分的に低下するだけで、Aβの量
が増加し、蓄積が促進されることを意味する。 |
| (4) |
ネプリライシンノックアウトマウスの脳内におけるAβ含量
は、海馬でもっとも高く小脳でもっとも低かった。これは、アルツハイマー病の病理像とよく相関する。さらに、McGeerら(University
of British Columbia)が我々の成果に基づいて、アルツハイマー病患者の脳におけるネプリライシンの発現を検討したところ、特に海馬で発現が低下していることを見出した報告ともよく一致している。 |
今後への期待
加齢に伴う脳内のネプリライシンの活性あるいは発現の低下がAβの量を上昇させ、アルツハイマー病を引き起こす可能性があることが示唆された。今後、以下のような発展が期待される。
| (1) |
新たな遺伝的危険因子の予測
ネプリライシンの遺伝子発現は、組織特異的に制御されている。神経細胞はタイプ1のmRNAを発現しているので、この発現制御に関わる遺伝子領域における変異や多型はアルツハイマー病の発症リスクに影響を与えると推測される。
|
| (2) |
危険因子の同定と除去による予防
ネプリライシンの発現や活性を低下させるものは危険因子となり得る。これらを同定し、除去することによって発症のリスクを抑えることができる。
|
| (3) |
活性あるいは発現の制御による発症の抑制
遺伝子治療あるいは遺伝子転写制御によって、脳内のネプリライシンの発現を選択的に上昇させることができれば、孤発性アルツハイマー病だけでなく家族性アルツハイマー病の発症を抑制することができると期待される。 |
| (4) |
発症前診断
脳の老化に伴ってネプリライシンの発現が低下するならば、その存在量を定量することによって各個人の発症リスクを事前に予測することができることが期待される。 |
おわりに
「生体内における個々の蛋白質の固有の寿命はどのようにして決定されるか?」という問いは、実は、日本のプロテアーゼ研究者が数十年にわたって取り組んできた命題である。したがって、本研究は、この生化学の伝統的命題に対する解答を得るための努力の一環でもある。
|
 |
 |
Aβ代謝と蓄積
Aβは定常的にアミロイド前駆体蛋白質(APP)から合成され、正常状態では速やかに分解される。産生の上昇、あるいは、分解の低下が蓄積の原因と考えられる。
|
Iwata, N., Tsubuki, S., Takaki, Y., Shirotani, K., Lu, B., Gerard, N.P., Gerard,
C., Hama, E., Lee, H.-J., Saido, T.C. (2001). Metabolic regulation of brain Aβ
by neprilysin. Science, 292, 1550-1552.
|
|
 |
 |
|
|