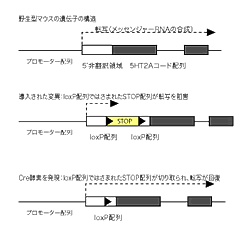
背景
神経伝達物質であるセロトニンの情報が次の神経細胞に伝わる際には、セロトニンが作用する受容体が必要です。このセロトニン受容体は10種類以上あり、それぞれの受容体は、生体内の違った機能をコントロールしていると考えられていますが、個々の受容体の機能分担についてはよく分かっていません。 不安行動に重要な役割を担う脳内の部位としては、大脳皮質、腹側線条体、海馬および扁桃体が知られています。これらの領野では、セロトニン受容体の一つである5-HT2A受容体が多く発現しており、5-HT2A受容体を介した情報伝達が、不安行動に関与していると考えられていました。このことから、 5-HT2A受容体の機能を欠損させたマウスを作成し、5-HT2A受容体と不安行動と関連を探ることとしました。
研究成果とその意義
実験の結果、5-HT2A受容体欠損マウスは、恐怖の条件付けや“うつ”関連行動に異常を示さないにもかかわらず、1つのリスク(不安)に対して、1つの選択肢しかない場合には、通常のマウスと違いがありませんでした。一方、2つ以上の選択肢があった場合、通常の野生型マウスであれば、葛藤の上、より低いリスク(不安)を選択しますが、 5-HT2A受容体を欠損させたマウスでは、葛藤もせず、高いリスクを選択するようになりました。 野生型マウスと異なるこの特徴は、大脳皮質でのみ5-HT2A受容体の発現を回復させることにより消失し、野生型マウスと同様に高いリスクを避ける行動を示しました。これらの結果は、リスクの高さを評価する能力について、大脳皮質がトップダウン制御するとのモデルを支持する成果です。人を含めた動物がリスクを適切に評価し、高いリスクを避けることは日常生活の中で重要とされる能力です。その一方で、大きな成果を得るためには、あえて高いリスクを冒すことも必要とされます。これをギャンブルとも表現します。つまりリスクは、時と場合によって選び分けなければならないものであることを考えると、この研究結果は興味深いものです。
今後の期待
セロトニン受容体の一つである5-HT1A 受容体を欠損するマウスでは、不安行動を増す方向に作用することが、今までの研究から報告されています。今回、5-HT2A受容体の欠損マウスでは、不安行動を減らす方向に作用することが示されました。 現在、うつなどの治療法に脳内セロトニン濃度を増加もしくは減少させる薬が利用されていますが、その効果は一定ではありません。その一因としては、セロトニン受容体の種類の多さがあげられます。今回、不安行動に関与する脳内の仕組みの一端が明らかになったことにより、不安や情動障害などの薬物治療に対して、より有効性の高い方法を確立できる可能性があります。また、受容体の機能を分子生物学的なアプローチを用い、脳内の局所ごとに詳細に解析する基礎研究は、今後、有効な治療法開発への道と考えられます。