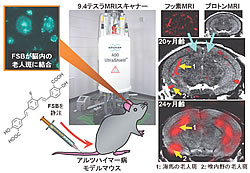
当研究チームは、アルツハイマー病に特異的な病理である老人斑アミロイドを、フッ素化合物とフッ素核磁気共鳴画像(MRI)を用いて生体モデルマウス脳において画像化することに成功しました。この技術は、アルツハイマー病の早期診断法開発に大きく貢献し、将来的には発症のメカニズム解明や、老人斑アミロイドを標的とした治療法の評価に役立つものと期待されます。
背景
アルツハイマー病は、老年期の認知症の中で最も頻度の高い疾患です。現時点におけるアルツハイマー病の大きな問題点は、患者さんが生きている間は確定診断がつかないことと、根本的な治療法が確立されていないことにあります。患者さんが亡くなった後で脳を病理学的に調べてみると、アルツハイマー病の場合老人斑と、神経原線維変化と呼ばれる2種類の病変が見出され、これらが確定診断の指標となっています。老人斑はアミロイドβ ペプチド(Aβ )が細胞外に蓄積した凝集物で、神経原線維変化はタウ蛋白が神経細胞内に沈着した病変です。アルツハイマー病では、Aβ やタウ蛋白はβ シートという2次構造をとることで線維状に自己凝集をきたします。これはアミロイド線維と呼ばれ、そのため老人斑や神経原線維などの病変は脳アミロイドと総称されます。近年の研究により、アミロイド病変はアルツハイマー病の臨床症状が出現するよりも20~30年も前の時点で、すでに脳内に現れ始めることが明らかにされています。したがって、生体の脳アミロイドを体外から検出することができれば、アルツハイマー病を発症前に診断することも不可能ではないと考えられます。また、脳アミロイドはただ単にアルツハイマー病の病理学的特徴であるのみならず、神経細胞の変性に密接に関わっていることも、さまざまな研究で示されています。そこで脳アミロイドの形成を阻害や分解促進によって、神経変性を抑え疾患を根本的に治療できると見込まれます。生体脳アミロイドの画像化が実現すれば、こうした治療法が脳アミロイドを減らしたり、出現をくい止めたりするのにどれだけ効果があるのかを、同一個体で時間を追って評価することが可能になるので、効率よく治療法開発を行えるようになります。
今回の成果
生体における老人斑の画像化は、これまでも放射性薬剤とポジトロン断層撮影などを用いて実現可能であることが示されてきました。しかしながら、放射性被爆や薬剤合成コストの問題などを考慮すると、 MRIによってアミロイドが可視化できる方が利点が多いと考え、当研究チームはMRIを用いた画像化法開発に取り組みました。一般的に普及しているMRIは、水素原子核(プロトン)の核磁気共鳴現象を利用しますが、プロトン以外にもフッ素原子などで同様の現象が見られます。したがって、フッ素を含有する薬剤を生体に投与してフッ素MRI撮影を行えば、薬剤の体内分布が画像化できます。元々フッ素は体内に存在しないので、ここで得られる信号は基本的にすべて薬剤に含まれるフッ素に由来することになり、高いコントラストで画像を得ることが可能です。そこで同仁化学研究所との共同研究により、フッ素を含有するアミロイド親和性化合物FSB※を新規に作成し、フッ素MRIへの応用を試みました。第一に、FSBが蛍光化合物であることを利用して、アルツハイマー病患者の脳切片や、Aβ が脳内に蓄積し老人斑が形成されるモデルマウスの脳切片を染色したところ、老人斑や神経原線維変化が蛍光で検出され、FSBが脳アミロイドに特異的に結合することが明らかになりました。第二に、モデルマウスに対してFSBの静脈内投与を行うと、FSBは脳内に移行して老人斑に結合することを、投与後に摘出した脳を顕微鏡で観察することで確認しました(図)。血液と脳組織の間には、血液脳関門と呼ばれる障壁があり、多くの薬剤はこの関門を通過できず脳へ移行しませんが、FSBは比較的分子量が小さく脂溶性が高いので、血液脳関門を通過し、脳内の老人斑に結合できると考えられます。第三に、FSBの静脈注射を行ったモデルマウスのフッ素MRIスキャンを実施したところ、海馬や嗅内野など老人斑が蓄積する部位に一致して、フッ素信号が検出されました(図)。この時使用した撮像装置は、マウス頭部の撮影用に設計された9.4テスラ高磁場・高分解能MRIスキャナーで、50~100ミクロンの微小な構造物を描出することが可能になっています(図)。また、マウスの月齢が増すにつれて老人斑が増加しますが、それに伴ってフッ素信号も増加することから、FSBとフッ素MRIにより老人斑をある程度定量的に評価できることが分かりました。
※:(trans,trans)-1-fluoro-2,5-bis-(3-hydroxycarbonyl-4-hydroxy)styrylbenzene
今後の期待
今回の研究でMRIを用いてマウス脳における老人斑が画像化できたことより、老人斑形成を抑えるような治療法をマウスに試みた際に、本法により治療効果を経時的に評価することが可能になると期待されます。さらに、老人斑の検出と同時に、脳容積計測による脳萎縮の評価などをMRIで行うことで、脳アミロイド蓄積のどの段階で神経変性が起こるのかを知る手がかりが得られ、アルツハイマー病発症の分子機構解明に大きく寄与すると考えられます。
現時点におけるフッ素MRIの問題点は、微量な薬剤の分布が分かるほど感度が高くないということです。本研究でもフッ素MRIスキャンを行う際に 20mg/kgという高用量でFSBを投与する必要があり、したがって現在の撮影法をすぐさまヒトの診断に応用することは困難です。しかしながら、より多くのフッ素原子を含むアミロイド親和性化合物の開発や、化合物の脳への移行を高める工夫、さらにはMR信号検出コイルの改良などの技術的進歩がなされることで、将来的には臨床診断にも応用が可能になると見込まれます。