研究チームは、重篤な知能障害を伴う難治てんかんを持つ患者さんにおいて変異が見られるナトリウムチャネル遺伝子に変異を導入した疾患モデルマウスを作成し、このマウスにおいて重篤なてんかん発作と抑制性神経細胞の機能異常が見られる事などを確認しました。更に、このチャネル蛋白は本来、特定の種類の抑制性神経細胞の軸索部等に多く発現し、興奮性神経細胞ではほとんど見られない事を見い出しました。この知見は、従来の当該チャネル蛋白の分布に関する通説を覆すものであり、てんかんが発症する仕組みの理解、治療法の開発などに大きく寄与するものです。
背景
てんかんは、神経細胞の過剰興奮によって引き起こされる発作を特徴とする、全人口の1%以上が発症する頻度の高い神経疾患です。てんかんには多数の種類があり、その過半数に遺伝的背景が想定され、実際に今まで複数の原因遺伝子が同定されています。その一つ、電位依存性ナトリウムチャネルαサブユニット1型蛋白をコードするSCN1A遺伝子では、重篤度の大きく異なる複数種のてんかんで既に200を超える数の疾患変異が報告されており、現在、このSCN1Aは今までに報告されたてんかん原因遺伝子の中でも、評価の確立した、最も代表的なものとなっています。SCN1Aにおいて変異が見いだされるてんかんの一つ、乳児重症ミオクロニーてんかんは、乳幼児期の熱性けいれんを初発症状とし、難治の強直間代発作とミオクロニー発作、重い精神発達障害を特徴とする重篤なてんかんで、実に約8割の患者さんでSCN1A変異が見いだされます。変異は約3分の2がナンセンスもしくはフレームシフトなどチャネル蛋白を分断する変異であり、約3分の1がミスセンス(暗号化されたアミノ酸が別のアミノ酸に変化する)変異です。電位依存性ナトリウムチャネルは神経細胞の興奮に主要な働きをする蛋白として知られておりますが、その(特にサブタイプごとの)機能については不明な部分も多く残されています。このSCN1AがコードするNav1.1が果たす本来の機能の詳しい解析と、その異常により引き起こされるてんかんの発症メカニズムの解明は、てんかんの理解と有効な治療法の開発にとっても非常に重要です。
今回の成果
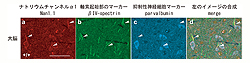
研究チームは、独立した3例の乳児重症ミオクロニーてんかん患者で見いだされたSCN1Aナンセンス変異(R1407X)を導入したマウスを作成し、詳細に解析しました。その結果、変異導入マウスにおけるNav1.1蛋白の消失、てんかん発症、抑制性神経細胞の機能不全等に加え、野生型マウスにおいてNav1.1タンパク質がパルブアルブミンと呼ばれるカルシウム結合蛋白が発現している特定の(パルブアルブミン陽性)抑制性神経細胞に発現していること、更にその軸索に多く発現することなどを複数の抗体と変異導入マウスをコントロールとした厳密な実験のもとに突き止めました。Nav1.1タンパク質は今まで興奮性および抑制性神経細胞の樹状突起および細胞体で発現しているとされてきましたが、今回のパルブアルブミン陽性抑制性神経細胞軸索などに限局した発現の発見は、それら以前までの報告を覆す知見であり、更に、乳児重症ミオクロニーてんかんなどSCN1A遺伝子変異によって引き起こされるてんかんの発症の原因がパルブアルブミン陽性細胞の機能低下により興奮性神経細胞の活動を抑制できなくなることに有ることを強く示唆するものとなりました。
今後の期待
今後、パルブアルブミン陽性抑制性神経細胞をターゲットとすることにより、現在では治すことが困難な重篤で悲惨なこれらてんかんの新しい治療法の開発に道が開けるものと期待されます。