研究の背景
ハンチントン病や遺伝性の脊髄小脳変性症の多くは、その病気の原因遺伝子のCAG塩基配列の繰り返しが異常に伸長することにより、異常に伸長したグルタミン鎖を含む原因遺伝子産物が神経細胞に異常蓄積し、神経細胞死や機能異常を引き起こす疾患です。異常に伸びたグルタミン鎖がその病気の発症に強く関わっていることから、ポリグルタミン病とまとめて呼ばれています。ポリグルタミン鎖の長さが長いと若年で発症することから、ポリグルタミンの長さに依存した神経細胞への毒性がどのようにして生じているかが、その病態を考える上で重要です。近年、そのような病態を再現するモデルマウスの解析から、ポリグルタミン病の神経細胞の核にポリグルタミンを含む蛋白凝集体:核内封入体が形成されることが分かり、これらの病気において凝集体形成が重要な役割を果たしていることが示唆されました。このようにポリグルタミン病はその病態が少しずつ分かってはきましたが、治療法が確立しておらず、遺伝子診断が直接患者さんの治療に結びつかないといった矛盾があり、治療法、発症予防法の確立が急がれていました。
研究の概要
われわれはポリグルタミンを発現する細胞モデルを用いて、伸長するポリグルタミンを発現すると異常な凝集体を形成し、シャペロン系がその凝集を抑制しようとするにもかかわらず、凝集抑制がうまくいかないと、細胞の蛋白分解系プロテアソームを阻害して細胞死を引き起こすという機序を明らかにしてきました。これらの病態の中核にあるのは凝集体形成であり、その凝集体にさまざまな分子がリクルートされることです。
このような病態の解析から、凝集抑制がこの病態を抑えるために必要と考え、最も上流のポリグルタミンを含む蛋白の構造異常の解析を行いました。ポリグルタミン鎖を安定性の極めて高い蛋白質で構造も明らかにされている蛋白質の一つであるミオグロビンへ挿入し、ポリグルタミン鎖の構造およびポリグルタミン挿入に伴う(ホスト)蛋白質の構造変化を検討しました。その結果、変異型ミオグロビンに挿入された伸長したポリグルタミン鎖は分子内ベータシート構造をとっていることが判明しました。また、35、50のリピート数を持つミオグロビンは凝集体を形成し始めると、分子間ベータシート構造を含んでいることが分かり、またポリグルタミンの伸長に伴いミオグロビンが不安定化することが示されました。そこでこの研究で用いた変異ミオグロビンの系を用いて病態の最も上流である凝集体形成を抑える化合物を検索しました。
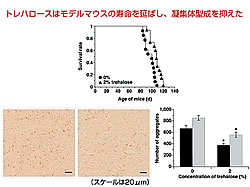
(図下左)核内封入体の減少(左:コントロール(比較対照群)、右:トレハロース服用)。
(図下右)核内封入体の定量(黒:8週令、灰:12 週令)
Mb-Q35(35ポリグルタミンを含むミオグロビン)を用いて200あまりの化合物をin vitroで検討したところ、二糖に凝集抑制効果が認められ、その中でもトレハロースが最も強力でした。そこでトレハロースの効果をポリグルタミンが発現した細胞においてみたところ、凝集抑制効果が認められ、トレハロース合成酵素OtsA、Bを発現したところ凝集抑制効果、細胞死抑制効果は、シャペロンの HDJ1と同程度に認められました。さらに、トレハロースのMb-Q35の不安定性に対する影響を評価したところ、トレハロース存在下でMb-Q35は正常域のQ12(12グルタミンを持つもの)と同程度になることが示され、これらの結果はトレハロースが分子を安定化し、凝集抑制効果があり、その結果細胞死抑制効果が認められたと考えられました。さらにハンチントン病モデルマウスR6/2マウスの飲料水に2%の濃度で投与したところ生存日数の増加(10% 程度)、ロタロッドテストなどの機能低下の遅延、病理学的な凝集体形成減少を認めました。以上の結果、トレハロースは伸長したポリグルタミンによるホスト蛋白の不安定化を抑え、凝集体形成を抑えることにより発症を遅延させたと考えられました。
研究の意義
本研究によって凝集体形成が病態の最も上流にあり、これを抑えることにより、病態の進行を抑えることが可能であることが示されました。この抑制効果が完全なものでないことは、より強力な抑制効果のある化合物の探索や、あるいは凝集体分解の促進などが今後の治療法開発にとって必要であることを示唆しています。アルツハイマー病、パーキンソン病あるいは筋萎縮性側索硬化症などの神経変性疾患の病態において、蛋白のミスフォールディングが注目されています。これらの疾患においても分子安定化による治療の可能性が示唆されたと考えています。